-拓达维®是首个能为既往接受过内分泌治疗、并至少接受过两种化疗的HR+/HER2-转移性乳腺癌患者带来总生存期获益的靶向Trop-2的抗体偶联药物-
*拓达维®尚未在国内获批用于治疗HR+/HER2-转移性乳腺癌,该适应症的安全性和有效性尚未确定。
2023年2月3日,吉利德科学宣布,美国食品药品监督管理局 (FDA) 已批准拓达维®(戈沙妥珠单抗)用于既往接受过内分泌治疗、并在疾病转移阶段至少接受过两种其它系统治疗的不可切除的局部晚期或转移性激素受体阳性、人表皮生长因子受体2阴性(HR+/HER2-)的乳腺癌成人患者,这些患者HER2的免疫组织化学(IHC)评分为0、1+或2+,且原位杂交(ISH)检测结果阴性。这一批准基于3期TROPiCS-02研究的数据,研究结果显示,患者的无进展生存期(PFS)和总生存期(OS)展示出具有统计学意义和临床意义的显著改善。此外,拓达维®被美国国家综合癌症网络®(NCCN®)发布的《肿瘤学临床实践指南》(NCCN Guide®)推荐为转移性HR+/HER2-乳腺癌患者的1类首选治疗方法。
美国加州大学旧金山分校
海伦迪勒家族综合癌症中心教授、
乳腺肿瘤与临床试验教学负责人、
TROPiCS-02研究的主要研究者
Hope Rugo博士表示:
尽管过去几十年里医学取得了进步,但经治HR+/HER2-转移性乳腺癌患者对新治疗选择的需求仍然存在。几乎所有此类乳腺癌患者最终都会对内分泌疗法产生耐药,而只能选择接受化疗。这项批准对乳腺癌患者至关重要。对于接受过内分泌疗法和化疗的患者,我们能够提供的治疗选择有限,能够有临床意义3个月以上的生存获益,并同时拥有相当的生活质量,对这些女性患者而言是非常有意义的。
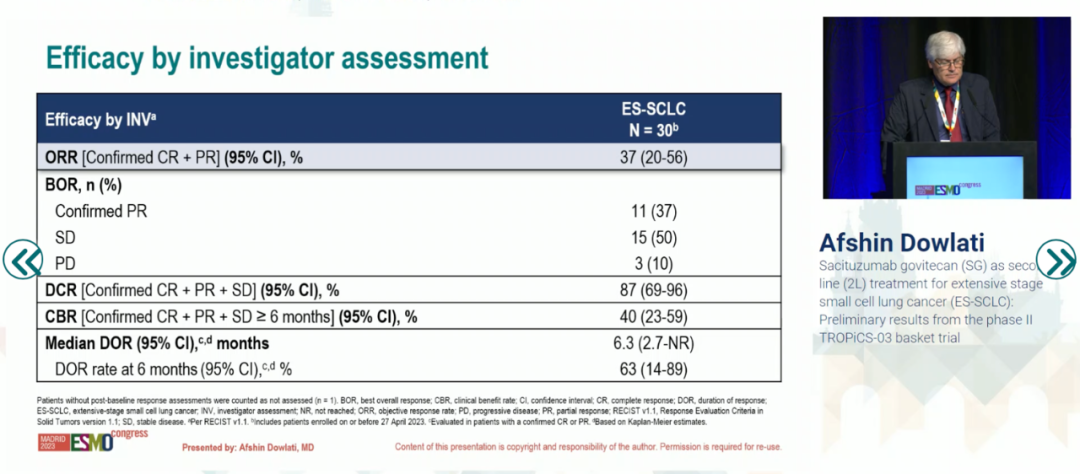
在TROPiCS-02研究中,与对照单药化疗(医生选择的治疗方案,TPC)相比,拓达维®组患者的总生存期(OS)展示出具有统计学意义和临床意义的显著改善(3.2个月)(中位总生存期:拓达维®组相较对照组=14.4个月/11.2个月;风险比[HR]=0.79; 95% CI:0.65-0.96; p=0.02)。拓达维®组患者在疾病进展或死亡风险上还呈现34%的下降 (中位无进展生存期:拓达维®组相较对照组=5.5个月/. 4.0个月;HR : 0.66;95% CI : 0.53-0.83 ; p=0.0003)。拓达维®组一年内无疾病进展的患者比例是化疗组的三倍(21% vs 7%)。在事后分析中,数据显示拓达维®在TROPiCS-02试验中对HER2低表达和IHC评分为0的经治转移性乳腺癌患者均展示出疗效。
拓达维®还显著改善了其他次要终点指标,包括基于EORTC-QLQ-C30的全球健康状况/生活质量及疲劳量表评估的客观缓解率和恶化时间(TTD)。在疼痛量表上未观察到恶化时间方面的显著统计学差异。
吉利德科学董事长兼首席执行官Daniel O'Day表示:“继拓达维®为转移性三阴性乳腺癌患者的治疗带来变革之后,我们很高兴看到拓达维®也能为经治HR +/HER2-转移性乳腺癌患者带来新的希望。我们感谢医务人员、患者及其家人对TROPiCS-02研究的信任,感谢他们为实现今天的这一里程碑提供的帮助。”
拓达维®的安全性与之前的研究一致,在该患者群体中未发现新的安全性问题。在TROPiCS-02研究中,最常见的严重不良反应(>1%)是腹泻(5%)、发热性中性粒细胞减少(4%)、中性粒细胞减少(3%)、腹痛、结肠炎、中性粒细胞减少性结肠炎、肺炎和呕吐(各2%)。在TROPiCS-02研究中,最常见的3-4级实验室异常(发生率≥25%)是中性粒细胞和白细胞的减少。接受拓达维®治疗的患者均未出现间质性肺疾病。
拓达维®的这项申请基于FDA的Orbis计划获得批准,并被FDA授予优先审评资格。
此外,欧洲药品管理局(EMA)已受理拓达维®的II类变更上市许可申请(MAA),用于HR+/HER2-转移性乳腺癌患者。
关于激素受体阳性/人表皮生长因子受体2阴性(HR+/HER2-)转移性乳腺癌
激素受体阳性/人表皮生长因子受体2阴性(HR+/HER2-)乳腺癌是最常见的乳腺癌类型,约占所有新发病例的70%。几乎三分之一的早期乳腺癌病例最终会发生转移,在HR+/HER2-转移性乳腺癌患者中,5年相对生存率为30%。随着HR+/HER2-转移性乳腺癌患者对内分泌治疗产生耐药性,她们的主要治疗选择仅限于单药化疗。在这种情况下,患者通常在整个治疗过程中需接受多线化疗方案,但预后仍较差。
关于TROPiCS-02研究
TROPiCS-02研究是一项全球性、多中心、开放标签的3期研究,以1:1的比例随机分组543名既往接受过内分泌治疗、CDK4/6抑制剂和二到四线化疗的HR+/HER2-转移性乳腺癌患者,研究旨在评估拓达维®与医生选择的化疗方案(艾立布林、卡培他滨、吉西他滨或长春瑞滨)相比的疗效。根据实体瘤疗效评价标准(RECIST 1.1),主要终点为无进展生存期,通过对接受拓达维®和化疗的患者进行盲态、独立、中心化评估(BICR)。次要终点包括总生存期、总缓解率、临床获益率和应答持续时间,以及安全性、耐受性和生活质量指标评估结果。在本研究中,根据美国临床肿瘤学会(ASCO)和美国病理学家协会(CAP)标准将HER2阴性定义为免疫组织化学(IHC)评分为0、1+或2+且原位杂交(ISH)检测结果阴性。关于TROPiCS-02研究的更多信息,请参见https://clinicaltrials.gov/ct2/show/NCT03901339。
关于拓达维®
拓达维®(戈沙妥珠单抗)是一款同类首创的抗体偶联药物,靶点为Trop-2受体,这是一种在许多类型肿瘤(包括超过90%的乳腺癌和膀胱癌)中均高表达的细胞表面抗原。拓达维®通过可水解的连接子将靶向Trop-2的单克隆抗体与有效载荷拓扑异构酶I抑制剂SN-38相连。这种独特的设计保证了在Trop-2表达细胞和邻近微环境中的有效活性。
拓达维®已在超过40个国家和地区获批上市,并正在多个其它国家和地区接受新药上市审评,用于治疗既往接受过至少两种系统治疗、且其中至少一种为针对转移性疾病的治疗的不可切除的局部晚期或转移性三阴性乳腺癌(TNBC)成人患者。
拓达维®还在美国获批用于部分经治HR+/HER2-转移性乳腺癌患者的治疗,并通过加速审批通道,获批用于部分转移性尿路上皮癌(UC)患者的二线治疗。
对于拓达维®其它潜在应用的研究也在进行中,这包括用于三阴性乳腺癌、HR+/HER2-乳腺癌、转移性尿路上皮癌的其他治疗人群,以及Trop-2过度表达的一系列肿瘤类型,包括转移性非小细胞肺癌(NSCLC)、转移性小细胞肺癌(SCLC)、头颈癌和子宫内膜癌。
关于吉利德科学
吉利德科学是一家生物制药公司,成立三十多年来,探索并实现了多个医学上曾认为不可能实现的突破,旨在为公众创造一个更健康的世界。公司致力于推动药物革新,以预防和治疗HIV、病毒性肝炎和癌症等可能威胁生命的疾病。吉利德在全世界超过35个国家和地区运营,总部位于美国加利福尼亚州福斯特市。
2017年,吉利德科学开始在中国的商业运营,致力于在病毒学及肿瘤学这些可危及生命的疾病领域为中国患者提供创新治疗手段及方案,创造更健康的中国。如今,我们已将慢性乙型肝炎、丙型肝炎及HIV防、治领域的九个全球领先的药物引入中国,其中,七个药物已被列入国家医保目录,让更多患者接受全球领先药物治疗,重回健康生活成为可能。